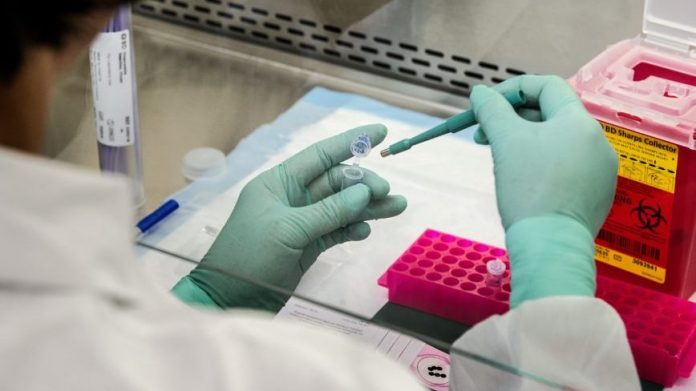
A Anvisa (Agência Nacional de Vigilância Sanitária) autorizou nesta 3ª feira (21.jul.2020) a empresa alemã BioNTech e a farmacêutica Pfizer a realizarem 1 ensaio clínico (testes de medicamentos em humanos) que estudará 2 tipos de vacinas contra a covid-19: BNT162b1 e BNT162b2.
Segundo a Anvisa, a autorização foi concedida depois de análise dos dados das etapas anteriores de desenvolvimento das vacinas, incluindo estudos não clínicos in vitro e em animais, bem como dados preliminares de estudos clínicos em andamento. A agência afirma que os resultados obtidos até o momento demonstraram 1 perfil de segurança aceitável dos medicamentos.
O estudo da BioNTech e da Pfizer estabelece a participação voluntária de cerca de 29.000 voluntários, sendo 1.000 no Brasil, distribuídos nos Estados de São Paulo e da Bahia. De acordo com a Anvisa, o recrutamento dos voluntários será de responsabilidade dos centros que conduzem a pesquisa.
Esta é a 3ª autorização para testes de vacina contra o novo coronavírus em humanos no Brasil. Em 2 de junho, a agência autorizou o ensaio clínico da vacina desenvolvida pela Universidade Oxford, no Reino Unido. Em 3 de julho, foi autorizado o estudo da vacina desenvolvida pela empresa chinesa Sinovac Research & Development Co. Ltd., em parceria com o Instituto Butantan.
As vacinas BNT162b1 e BNT162b2 são baseadas em ácido ribonucleico (RNA), que codifica 1 antígeno específico do vírus Sars-CoV-2, o novo coronavírus. O RNA é traduzido pelo organismo humano em proteínas que depois irão induzir uma resposta imunológica.
O ensaio clínico terá fase 1,2 e 3, controlado com placebo, randomizado, cego para o observador, de determinação de dose, para avaliar a segurança, a tolerabilidade, a imunogenicidade e a eficácia das vacinas em adultos. O ensaio clínico é composto por 3 estágios e o Brasil participará do estágio 3, que corresponde às fases 2 e 3 do estudo.
Em entrevista ao Poder em Foco, programa do Poder360 em parceria editorial do SBT, em 21 de maio, a diretora médica da Pfizer, Márjori Dulcine, disse que a empresa farmacêutica estima fabricar milhões de doses da vacina contra a covid-19 já a partir de outubro deste ano. A produção em larga escala, no entanto, só deve ocorrer em 2021.
Márjori Dulcine disse ainda que a vacina será similar à usada para combater a gripe, sendo aplicada com uma agulha intramuscular.
A diretora médica da Pfizer explicou também as dificuldades para a criação de uma vacina. Normalmente, pode durar de 10 a 15 anos. A que será usada contra o coronavírus deve ser desenvolvida em tempo recorde.
“Nós estamos falando de uma vacina poder ser produzida e estar disponível em meses, em menos de 1 ano. A Pfizer, junto com a BioNTech, começou essa pesquisa no final de fevereiro. Em março, houve a 1ª aplicação da dose em 12 participantes na Alemanha. Agora, no início de maio, começou a aplicação nos Estados Unidos.”
DESENVOLVIMENTO DE VACINAS
Pesquisadores correm contra o tempo para achar uma vacina contra o coronavírus. De acordo com relatório (341 KB) divulgado pela OMS, há 158 iniciativas para se formular uma substância que imunize contra o vírus. Vinte e uma delas estão em testes clínicos, ou seja, com humanos. É o dobro do que havia no começo de junho, quando 10 tinham iniciado os testes.
A maior parte das 21 substâncias testadas está nas fases 1 ou 2, que verificam segurança, toxidade e se há alguma resposta imune. Há duas delas que iniciaram a fase 3 –a última antes da liberação para a produção. São as vacinas da Atrazeneca (Reino Unido) em parceria com a Universidade Oxford; e da Sinovac (China). As duas farmacêuticas firmaram acordo de produção em parceria com o Brasil.
Estudos indicam que menos de 10% das drogas que entram em estudos clínicos acabam aprovadas pela FDA (agência do Departamento de Saúde dos EUA, responsável pela liberação de alimentos e medicamentos na indústria farmacêutica).
Saiba nos infográficos abaixo como é o processo de desenvolvimento das vacinas e quais são aquelas com maiores chances de ter a produção em massa iniciada rapidamente. O grande número de candidatas não significa, necessariamente, uma chance alta de que várias serão aprovadas.